Морфологическая верификация: определение термина, особенности
Предположить характер новообразования в организме можно благодаря клиническим и рентгенологическим симптомам, а вот определить его гистогенетическую принадлежность можно только благодаря морфологической верификации диагноза. Основной задачей такой диагностики является перепроверка онкологического диагноза для его подтверждения и подбора эффективного курса химиотерапии.
Морфологическая верификация

Услышав впервые от доктора о необходимости проведения морфологической диагностики, многие не имеют представления, что это и для чего проводится.
Верификация является важным исследованием, без которого невозможно принять решение о дальнейших действиях. Морфологическая верификация — это медицинская процедура, которая помогает подтвердить или опровергнуть онкологический диагноз. Чтобы провести исследование, необходимо получить материал. Его выбор в основном зависит от локализации образования. После проведения исследования специалист в зависимости от результата определяет дальнейшую тактику лечения, которая может быть консервативной или хирургической. Только после морфологического подтверждения может планироваться адекватное лечение. Показанием для проведения верификации являются объемные образования или диффузные изменения органа или его структур. Для проведения морфологического исследования забор ткани осуществляется следующим образом:
- при поверхностных изъявленных опухолях берется соскоб и мазки-отпечатки;
- при неглубоко размещенных узловых образованиях проводится пункция;
- при невозможности взятия пункции проводится биопсия с забором участка ткани;
- после неудачных попыток верификации всеми перечисленными выше методами проводится открытая биопсия.
Морфологическая верификация диагноза практически ничем не отличается от цитологической пункции. Чтобы взять материал на исследование, сначала человеку проводят анестезию мягких тканей и кожного покрова, после этого выполняется незначительный разрез кожи, через который внедряется специальный инструмент в мягкие ткани и непосредственно в ткань опухоли. Все последующие действия напрямую зависят от используемого прибора.
Методы верификации
Стандартным вариантом гистологической верификации диагноза является забор тончайших срезов биопсийных тканей для последующего микроскопического исследования. Благодаря им получается полезная информация о составе опухоли.
Морфологическая верификация опухоли проводится следующими способами:
- гистохимией;
- иммуногистохимией;
- иммунофлюоресценцией;
- иммуноферментным анализом.
Независимо от того, какая методика для проведения исследования будет выбрана, целью верификации является не только определение разновидности опухоли, но и оценка клеточных модификаций. По результатам исследования появляется возможность безошибочно принять решение и выбрать тактику лечения.
Гистохимическое исследование

С помощью гистохимической методики можно получить ценную информацию о функциональной активности образования, его типе и гистогенезе. Данный метод позволяет точно поставить диагноз и решить вопрос его дифференциальности.
В расположении гистохимии находятся многочисленные реакции, которые оказывают содействие выявлению разных классов веществ.
Иммуногистохимия
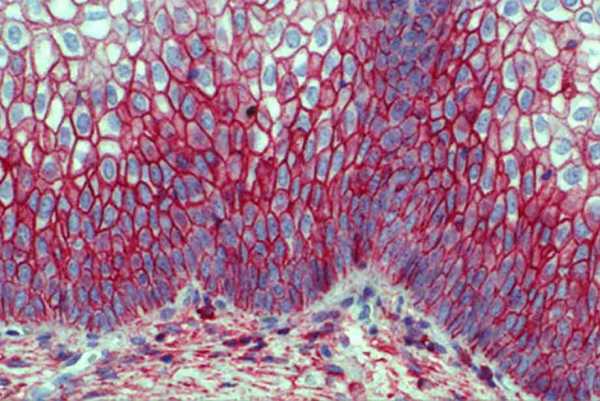
ИГХ является методом визуализации, который помогает определить локализацию веществ в препаратах тканевых срезов. В основе данного метода лежит принцип характерного взаимодействия антигенов с антителами, полученными особенным методом.
Иммунофлуоресценция
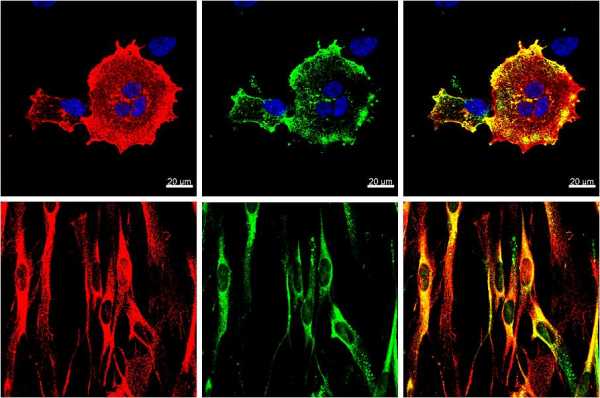
Метод исследования основан на чувствительности флюоресцентной микроскопии и специфичности иммунологической реакции. В процессе его проведения опухолевая ткань метится специальным красителем, который помогает доктору точно определить диагноз. Особенностью этого метода является простота и необходимость использования минимального количества изучаемого материала.
Иммуноферментный анализ
Метод диагностики обладает высокой восприимчивостью и позволяет устанавливать минимальные количества вещества. В современных методах диагностики именно с помощью этого способа определяется локализация антигена. Для проведения анализа используются специальные ферменты для обнаружения рака.
Независимо от выбранной методики целью любого морфологического исследования считается точное определение типа опухоли и оценки изменений на клеточном уровне. Можно сказать простыми словами, что морфологическая верификация — это определение разновидности опухоли и ее запущенности для правильного выбора тактики лечения.
Методы получения материала для морфологического исследования
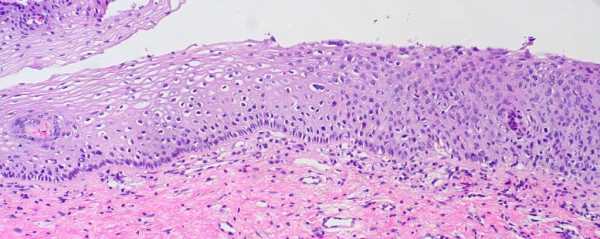
Для морфологической верификации диагноза необходимо получить материал. Сделать это можно следующими способами:
- Трепан-биопсия – считается одной из самых результативных процедур, несмотря на то что имеет определенные недостатки. Для взятия материала используются специальные иглы с внутренними режущими механизмами. С их помощью получается столбик ткани из опухоли. Этот метод позволяет провести морфологическую верификацию молочных желез, предстательной железы, легкого, печени, позвоночника и лимфатических узлов.
- Инцизионная биопсия – самый популярный метод, который выполняется с помощью скальпеля, которым берется материал из центра подозрительных участков, по периферии опухоли. При этом обязательно нужно делать это вне зон отека, некроза и кровоизлияния грануляционной ткани.
- Эксцизионная биопсия – суть такого метода заключается в полном радикальном удалении опухоли. Этот способ применим только если новообразование имеет небольшие размеры. В таком случае этот способ наиболее предпочтителен, так как имеет как диагностическое, так и терапевтическое значение.
Выбор способа морфологической верификации определяет лечащий врач в зависимости от особенностей сложившейся ситуации.
Последовательность морфологических изменений
Что это такое морфологическая верификация диагноза, и в какой последовательности происходят изменения в процессе развития рака, знают не многие. К сожалению, в основном люди начинают интересоваться подобной информацией, только когда сталкиваются с проблемой.
Онкология в процессе развития проходит определенные стадии, и в результате проведения морфологической верификации доктор может наблюдать разные нюансы развития. При верификации могут обнаруживаться следующие изменения в тканях:
- диффузная и очаговая гиперплазия – процесс не опасный и обратимый;
- метаплазия – доброкачественное новообразование;
- дисплазия – предраковое образование;
- рак in situ – преинвазивное раковое поражение;
- микроинвазия;
- прогрессирующий рак с метастазированием.
Промежутки времени между перечисленными этапами индивидуальны и в каждом отдельном случае могут варьироваться от нескольких месяцев до десятилетий.
Главной задачей морфологической диагностики является установление тканевой принадлежности опухоли. При этом выявляется не только ее наличие и разновидность, но и скрупулезно оценивается степень атипии клетки и нарушение тканевых структур. Чаще всего проводится морфологическая верификация щитовидной железы, молочной, предстательной, печени, почек и позвоночника. Метод проведения исследования в каждом отдельном случае определяется персонально.
fb.ru
33. Способы верификации диагноза рака и оценки распространенности опухолевого процесса.
Верификация — путем исследования биоптата. Это мб кусочки тканей, экскреты, секреты, мазки-отпечатки, соскобы, пунктаты. Методы: морфологические и цитологические. Морфологический: материал тканевой, дает заключение о гистогенезе, степени распространения опухоли. Оценка распространенности: определяют наличие прорастания опухоли в кровеносные и лимфатические сосуды, опухолевых клеток в просветах сосудов, распространение опухоли по периневральным и периваскулярным пространствам, прорастание ее в окружающие органы и ткани.
Цитологический: материал – отдельные клетки или группы клеток, не позволяет судить о степени распространения опухоли, не всегда может определить гистологическую форму. Преимущества: больше информации о структуре и функции клеток, возможно неограниченное повторение процедур, доступность для исследования всех органов, возможно обнаружить диспластические состояния и самые начальные стадии рака.
34. Способы забора материала для верификации диагноза злокачественного новообразования.
Для морфологического исследования:
1.трепан-биопсия – специальные иглы с внутренним режущим механизмом. Недостатки: маленький кусочек ткани, возможность имплантации опухоли по ходу иглы. Гистология. Выполняют при: раке предстательной железы, средостения, молочной железы, периферическом раке легкого с инвазией плевры, метастазах рака в печень, при опухолях позвоночника, при исследовании лимфоузлов.
2.инцизионная биопсия – с помощью скальпеля, материал берется в пределах опухоли из центральных и периферических участков опухоли, вне некроза, грануляции, отека, кровоизлияния. Глубина не менее 2-3мм. Гистология.
3.эксцизионная биопсия – полное радикальное удаление опухоли при её небольших размерах вместе с участком окружающей тани. Удаление материала одним блоком. Гистология.
4. интраоперационная биопсия – срочная, 20 минут. На замороженных срезах. Не рекомендуется отправлять лимфоузлы при подозрении на злокачественную лимфому,т.к. точный ответ можно получить только на парафиновых срезах (4-5 дней).
Для цитологического исследования:
-Для эксфолиативной цитологии – отстаивание биологической жидкости, из полых органов можно получит смывом.
Мазки-отпечатки или соскобы.
-Для неэксфолиативной (пункционной, аспирационной) цитологии – клетки из опухоли аспирированы при пункции иглой. (лимфоузлы, костный мозг,щит.ж-за и т.д.)
Так же экссудаты и транссудаты из замкнутых полостей.
-Эндоскопическая цитология – прицельный забор во время эндоскопии. !первая биопсия берется из самого измененного участка,т.к.затем появляется кровоточивость и следующие могут быть менее точными!!
-Прицельная пункция под контролем УЗИ, КТ.
35. Методы специального лечения в онкологии. Классификация, общая характеристика.
а) хирургическое
б) лучевая терапия
в) лекарственная терапия системного действия:
-химиотерапия
-гормонотерапия
Г)сопроводительная (поддерживающая) терапия – позволяет предупредить или уменьшить побочные эффекты лекарственной и лучевой терапии, уменьшить клинические симптомы тяжелых осложнений, обусловленных распространенным опухолевым процессом.
д) комбинированный – хирургическое + лучевое / лекарственное лечение
е) комплексный – лучевое + лекарственное
ж) сочетанный – два варианта одного метода (например, внутритканевая + наружная лучевая терапия)
— Радикальное лечение: полная ликвидация всех очагов опухолевого роста.
— Паллиативное лечение: излечение заведомо недостижимо. Цель: уменьшение массы и задержка роста опухолевых очагов и таким образом продление жизни больного на более или менее длительный срок при лучшем её качестве.
— Симптоматическое лечение: только устранение или ослабление проявлений заболевания и его осложнений.
Классификация хирургических вмешательств:
1. – радикальные:
*типовые (одним блоком +регионарный лимфотич.аппарат), *комбинированные (пораженный орган + полностью или частично соседние органы, на которые распространилась опухоль. Применяется если нет отдаленных метастазов)
* расширенные (границы лимфодиссекции значительно шире)
*экономные и органосохраняющие
2. –симультантные (одновременное удаление опухолей различной локализации)
3. –паллиативные. Циторедуктвные – разновидность паллиативных.(удаление основной массы опухоли, на ее остаток будетдействовать лекарственное лечение)
4.-повторные second-look (полное удаление опухоли после лекарственной терапии, когда во время первой опериции была неоперабельна или удалена частично)
5.-диагностические
6.-эксплоративные (проработанные) – в ходе интраоперац.ревизии обнаружены неудалимые метастазы. Т.е. в результате ничего не удалено.
7.-симптоматические
8.-реабилитационные (пластические, косметические, восстановительные)
Лучевая терапия: при помощи ионизирующих излучений.
Источники излучения:1. Искусственные или естественные радионуклиды
2. Электрофизические аппараты (бетатрон, рентгеновские аппараты, линейные ускорители электронов)
методы облучения:
А) дистанционная терапия (телетерапия)
1. гамма-терапия
2. электронное и тормозное излучение
3. корпоскулярное излучение
4. короткофокусная рентгенотерапия
Каждый из методов может быть статическим или динамическим.
б) контактные методы(брахитерапия):
*аппликационное
*внутреннее облучение:
1. внутриполостное
2. внутритканевое
3. системное
Химиотерапия опухолей. Лек.препараты, тормозящиепролиферацию или необратимо повреждающих злокачественные клетки.
Основные группы лекарственных противоопухолевых препаратов
:1. Алкилирующие препараты: циклофосфамид, иофосфамид
2. Антиметаболиты: цитарабин, метотрексатю
3. противоопухолевые Антибиотики:доксорубицин, блеомицин
4. алкалоиды растительного происхождения: подофиллин, винкристин
5. Производные платины: цисплатин, карбоплатин,
studfile.net
Диагностика. Верификация диагноза — Портал о скорой помощи и медицине
А. Верификация диагноза
1. Биопсия. Морфологическая верификация диагноза — основа диагностики и лечения. Опухоль и доброкачественные изменения (например, воспалительные) бывает сложно отличить одно от другого. Для биопсии выбирают наиболее доступный очаг: при этом ниже риск осложнений и выше вероятность получить материал. Для фиксации образцов используют раствор (например, В5), позволяющий выполнить иммуногисто-химический анализ, что необходимо при лимфоме и метастазах из невыявленного первичного очага.
Морфологические признаки опухолей, включая иммунофено-тип, указаны в Приложениях В-1, В-2 и В-3. Важную роль в диагностике опухолей играет иммунопероксидазный анализ (гл. 20, п. И.Б.4).
Ограничения метода. Определение типа опухоли и ее злокачественности не бывает абсолютно точным: ошибка может произойти во время взятия, обработки и исследования образца опухоли. Не вполне отчетлива грань между дисплазией и раком. Естественное течение многих опухолей переменчиво. Некоторые опухоли выглядят доброкачественными, но текут как злокачественные, и наоборот. Поэтому гистологический диагноз следует рассматривать в контексте клинической картины, анамнеза, физикальных и лабораторных данных.
Рекомендации
а. Не путайте возможность назвать опухоль с возможностью предсказать прогноз.
б. Не рассматривайте гистологический диагноз как непреложную истину.
в. Не полагайтесь на словесное заключение, кто бы его ни делал.
г. Обсуждайте с патологоанатомом клинические данные.
д. Убедитесь, что материала биопсии достаточно для стандартного исследования и специальных окрасок.
е. Если гистологический диагноз не соответствует клинической картине, предпримите следующие шаги:
1) проверьте, что материал получен от вашего больного;
2) пересмотрите препараты вместе с патологоанатомом;
3) если вопрос не снят, получите заключение в другом учреждении или повторите биопсию.
Опухолевые маркеры играют роль в диагностике некоторых опухолей. Изучалось множество маркеров, но лишь немногие применяются в клинике (табл. 1.2). Среди маркеров часто встречающихся опухолей только эстрогеновые рецепторы и белок ЕгЬВ2 (Her2/neu) при раке молочной железы позволяют предсказать эффективность лечения. 1. Терминология
а. Чувствительность — это доля больных, у которых уровень маркера повышен.
б. Специфичность — это доля здоровых, у которых уровень маркера в норме.
в. Предсказательная ценность положительного результата —вероятность опухоли у человека с повышенным уровнем маркера.
г. Предсказательная ценность отрицательного результата —вероятность отсутствия опухоли у человека с нормальным уровнем маркера.
д. Распространенность. Вероятность того, что повышение уровня маркера действительно вызвано опухолью, резко повышается, если в обследуемой группе доля больных велика. Уровень маркера более информативен, если его определять у больных, у людей с факторами риска или при рентгенологических данных, указывающих на опухоль.
www.03-ektb.ru
Гистологическая верификация опухоли
- Просмотров: 8741

Гистологическая верификация опухоли: методология, назначение, необходимость
Верификация опухоли – это медицинская процедура, целью которой служит перепроверка и подтверждение онкологического диагноза. В виду того, что к онкология – это отдельный раздел современной медицины, который изучает не только злокачественные, но и доброкачественные образования, гистологическая верификация опухоли нужна для определения ее типа и разработки плана дальнейшего обследования и лечения.
Гистологический диагноз определяет характер и тип опухоли, дает исчерпывающую и категоричную информацию, которая необходима для назначения правильного и эффективного курса лечения.
Методика гистологического исследования
Материалом исследования служит гистологический препарат – кусочек опухоли, нанесенный на стекла. Его извлекают при помощи определенной медицинской процедуры – биопсии. Полученные материалы подвергают лабораторным исследованиям – гистологическому, или – иммуногистологическому анализу. С помощью различных химических препаратов выявляют характер образования – доброкачественное или злокачественное, и его тип.
Преимущества и необходимость гистологической верификации опухоли
- Способы визуального исследования (рентгенография, КТ, МРТ и другие) не дают информации о характере опухоли – подтвердить доброкачественное или злокачественное образование может только гистологический анализ.
- Из всех диагностических методов гистологический анализ является самым достоверным и важным методом.
- Без данных исследования гистологического анализа агрессивные методы лечения (химиотерапия, лучевая терапия) не назначаются.
- Гистологический анализ позволяет вынести 100% диагноз, спрогнозировать дальнейшее течение болезни и принять решение о методах лечения, в том числе – оперативного вмешательства и его объемов.
- Гистологический анализ позволяет определить локализацию опухоли.
Порядок проведения гистологического анализа требует долгой и кропотливой работы. Поэтому он может проводиться только высококвалифицированным специалистом, имеющим необходимые знания в исследуемой области.
Итогом исследования является выдача соответствующего заключения, которое экономит время врача и пациента и сокращает объем дополнительных диагностических методов, а также упрощает выбор эффективного лечения. Кроме того, материалы биопсии можно использовать неоднократно – для перепроверки диагноза в других клинических лабораториях.
onkostrahovanie.ru
ВЕРИФИКАЦИЯ — Проблема верификации в доказательной медицине
Виноградов М.А. Московская медицинская академия имени И.М. Сеченова
Термин «медицина, основанная на доказательствах» или «доказательная медицина» (evidence based medicine) появился в лексиконе современных медицинских специалистов совсем недавно, однако за сравнительно небольшой период времени, основные принципы, вкладываемые в значение этого термина, составили доминирующую идеологию медицины XXI века. Возможно, это произошло потому, что современная клиническая медицина увидела в медицине «доказательной» возможный способ выхода из кризиса, в котором она находится с середины ХХ века. С помощью «доказательности» появилась возможность если не сделать медицину точной наукой, то по крайней мере, приблизить её к таковой.
Определение, данное в 1993 году Рабочей группой по доказательной медицине, звучит так: «Доказательная медицина – это раздел медицины, основанной на доказательствах, предполагающий поиск, сравнение и широкое распространение полученных доказательств для использования в интересах больных». Таким образом, доказательная медицина является новым подходом, к технологиям сбора, анализа, обобщения и трактовки медицинской информации. Внедрение принципов доказательной медицины в практику здравоохранения предусматривает оптимизацию качества медицинской помощи с точки зрения безопасности, эффективности, стоимости и др. В узком смысле, задача доказательной медицины, – преобразовать результаты научных исследований в конкретные клинические рекомендации для врачей.
Важным аспектом доказательной медицины стало установление степени достоверности и значимости, т.е. «доказательности» медицинской информации. Значимость любого медицинского исследования определяется рядом факторов, среди которых особое место принадлежит научному обоснованию этого исследования и возможности практического применения его результатов. По мнению ряда авторов, именно эти два фактора и составляют основу доказательной медицины [1].
Научная обоснованность медицинского исследования является мерой доверия к его результатам. Стандарты научной обоснованности включают строго определенные требования к проведению исследования, обработке его результатов и оценке достоверности. Необходимость создания единого подхода к оценке результатов медицинских исследований привела к выработке единых критериев научной обоснованности. На данный момент в литературе, посвященной доказательной медицине, можно встреть подробные алгоритмы оценки достоверности результатов клинических исследований [1]. Считается, что на основе этих результатов врач должен основывать свои клинические решения, пока в его распоряжение не поступят новые, более совершенные данные: «Какова бы ни была сила наиболее надежного из имеющихся фактов, врач должен брать его за основу для действий, будучи в то же время готовым к переоценке фактов» [Цит. по 1].
Можно утверждать, что доказательная медицина является логическим продолжением и этапом развития традиционной клинической медицины Запада, ориентированной на принципы позитивизма – философского направления ХХ века, оказавшего огромное влияние на современную науку.
Позитивизм ставит во главу угла тот постулат, что все подлинное, положительное («позитивное») знание о действительности может быть получено лишь в виде результатов отдельных специальных наук или их «синтетического» объединения. Согласно этому принципу, традиционная клиническая медицина обосновывала диагноз исходя из совокупности проанализированных данных, полученных различными дополнительными методами, заимствованными из различных отраслей науки – физическими, химическими, биологическими и т.д. С развитием современных технологий медицинской визуализации, физико-химического анализа, на второй план отошел собственно сам сбор анамнеза, который по сути своей, стал формальностью.
Антитеоретическая направленность позитивизма привела к появлению устойчивого мнения о том, что «настоящая» наука может опираться только на факты, а теория должна служить лишь для систематизации и классификации этих фактов. Отсюда убеждение, что на основании методов клинического наблюдения можно сделать лишь отдельные умозаключения о фактах, но не обобщенные гипотезы. Недостаток теоретических обоснований традиционной медицины привел к появлению многочисленных бесполезных и даже противоречащих принципам логики классификаций, а следование методологическим традициям позитивизма привело к явлениям классического атомизма, ассоциационизма, механицизма и крайнего эмпиризма в медицине. В качестве примера можно привести классические учебники, в которых патология базируется на разделении её на элементы (атомизм), существующие отдельно или соединенные друг с другом по принципу ассоциации (ассоциационизм). Для воплощения идеи, требующей исходить из данного в опыте, применяется метод клинического наблюдения, который должен стать непосредственной проверкой отдельных суждений («атомов» знания) путем сравнения с элементарными единицами опыта (эмпиризм) [6].
Накопление больших массивов данных в результате многочисленных клинических исследований привело к избытку частной информации, находящейся в «теоретическом» вакууме. Можно сказать, что клиническая медицина стала проявлять типичные симптомы ненаучности: избыток фактов и недостаток теории. Ведь суть науки в систематической интеграции данных, а не только в регистрации фактов. Потребность в объяснении накопленных данных вызвала усилия, направленные на создание небольших теорий на очень низком уровне обобщения. Эти отрывочные теоретические концепции малоприменимы даже при интерпретации даже узкой проблематики, так как ведут не к согласованности фактов, а скорее к росту числа новых концепций [6].
Попытки создания серьезных научных теорий с высоким уровнем обобщений явили ещё одну проблему – отбор эмпирических фактов, подтверждающих данную теорию. Следует отметить, что массив накопленных медициной теоретических фактов весьма неоднороден. Он включает исследования как правильно спланированные и выполненные с соблюдением всех требований в строго контролируемых условиях, так и работы, в которых требования к планированию и проведению строго не соблюдались. Тем не менее, оба вида исследований представляют собой научные факты. Для того, чтобы теория имела все признаки «доказательности», факты, отобранные для её подтверждения должны выдержать строгую проверку (верификацию с позиций доказательной медицины) на предмет научной обоснованности. Считается, что только массив эмпирических данных, единых по своим характеристикам (требования к проведению исследований, оценке результатов и достоверности) может стать научной базой для выдвижения той или иной теории. Именно принцип верификации философии позитивизма взяла на вооружение доказательная медицина, правда, придав ему несколько другое значение. Этот принцип в доказательной медицине четко не сформулирован, но рекомендации для определения «доказательности» научных исследований, предлагаемые экспертами доказательной медицины, являются ни чем иным, как верификацией.
Интересно, что впервые критерии верификации для определения роли инфекционного агента как причины болезни были четко сформулированы Робертом Кохом в 1882 году, т.е. до появления собственно философии позитивизма. Выдвинутая им гипотеза о том, что каждая болезнь имеет одну причину, а конкретная причина вызывает одну болезнь, подтверждалась следующими «протокольными постулатами»:
- Микроорганизм должен быть обнаружен в каждом случае заболевания.
- Микроорганизм должен быть выделен в виде чистой культуры.
- Микроорганизм должен вызывать специфическое заболевание при введении животному.
- Микроорганизм должен быть выделен у больного животного и идентифицирован.
Данный подход способствовал существенному развитию понятия причины в медицине. Постулат о том, что конкретный микроорганизм является причиной заболевания, послужил основой для многих открытий. Однако, для установления большинства болезней недостаточно одних постулатов Коха. Особенно при верификации гипотез заболеваний с множественными, неинфекционными факторами риска.
Формулирование гипотезы предшествует началу любого исследования. Формирование массива данных, служащих для её подтверждения, происходит по следующему примерному алгоритму верификации:
- Вначале разрабатываются критерии поиска информации (статей). Эти критерии представляют собой скрининговый метод отбора необходимой информации. Поиск может осуществляться по ключевым словам, словосочетаниям, фамилиям авторов и т.п. в доступных базах клинических данных (MedLine, Adonis, Cochrane Library).
- Из полученного массива данных необходимо исключить нерелевантные статьи, т.е. информацию не соответствующую критериям поиска. Для этого необходимо изучить название и абстракт статьи, так как контекст использования ключевых слов может быть различен.
- Информация в полученном массиве данных должна быть ранжирована по степени достоверности на основании существующих соглашений медицинской статистики (P?0.95, p?0.05) и критериев достоверности, предложенных экспертами доказательной медицины. Согласно мнению Шведского совета по методологии оценки в здравоохранении, достоверность доказательств из различных источников не одинакова, и зависит от типа проведенного исследования. Достоверность убывает в таком порядке:
- Рандомизированное контролируемое клиническое испытание;
- Нерандомизированное клиническое испытание с одновременным контролем;
- Нерандомизированное клиническое испытание с историческим контролем;
- Когортное исследование;
- «Случай-контроль»;
- Перекрестное клиническое испытание;
- Результаты наблюдений.
- Центр доказательной медицины в Оксфорде, предлагает следующие критерии достоверности медицинской информации:
- Высокая достоверность – информация основана на результатах нескольких независимых клинических испытаний с совпадением результатов, обобщенных в систематических обзорах.
- Умеренная достоверность – информация основана на результатах по меньшей мере нескольких независимых, близких по целям клинических испытаний.
- Ограниченная достоверность – информация основана на результатах одного клинического испытания.
- Строгие научные доказательства отсутствуют (клинические испытания не проводились) – некое утверждение основано на мнении экспертов.
- Исследователем должно быть четко определено отношение к информации с низкой степенью достоверности. Она может исключаться или не исключаться из исследования, но в любом случае это должно быть особо оговорено.
- На последнем этапе верификации осуществляется анализ содержания отобранных статей, чтобы отсеять те, которые не соответствуют сформулированной в начале исследования гипотезе.
На каждом из этих этапов имеется ряд факторов, оказывающих влияние на ход верификации, и в конечном итоге способных вызвать искажение результатов. Например, на этапе поиска информации могут быть найдены не все значимые источники по интересующей теме из-за плохого индексирования или нежелания фирм-спонсоров публиковать отрицательные результаты клинических испытаний. Сложности корректной трактовки, связанные с различиями в подходах, стандартах и способах оценки также могут оказывать влияние на результат.
Но возможно, что именно в виде подобного алгоритма, доказательная медицина представляет себе логико-методологический анализ медицинского знания, цель которого – формирование базы эмпирических данных в виде фактов науки, представленных языком, не допускающим двусмысленности.
Однако, необходимо отметить, что принцип верификации в философии позитивизма продемонстрировал свою ограниченность, так как наука в основном имеет дело с идеализированными объектами, которые не могут быть верифицированы.
Ограниченность метода верификации особенно заметна при попытке анализа воздействий внешней среды на здоровье человека, где многие факторы находятся в тесной взаимосвязи друг с другом, а степень риска других факторов не установлена. В данном случае результаты верификации могут быть представлены в виде «есть эффект» — «эффект отсутствует» на различных уровнях воздействия в рамках сформулированной теории о факторах риска. Формирование базы эмпирических данных в контексте социально-гигиенического мониторинга является основой для процесса принятия решений в управлении рисками. Основной же проблемой при верификации степени риска факторов внешней среды будет поиск и оценка достоверности данных с позиций медицинской статистики.
Подводя итоги, можно сделать заключение, что принцип верификации в доказательной медицине является мощным инструментом установления научной значимости выдвигаемых гипотез. Однако, при его использовании необходимо учитывать, те недостатки, которые обозначили критики позитивизма. В ряде случаев, например, при оценке факторов с окончательно не установленным значением, принцип верификации может стать основополагающим в создании научных теорий.
Литература
- Флетчер Р., Флетчер С., Вагнер Э. Клиническая эпидемиология. Основы доказательной медицины. Пер. с англ. – М.: Медиа Сфера, 1998. – 352 с., илл.
- Эволюционная эпистемология и логика социальных наук: Карл Поппер и его критики. Составление Д.Г. Лахути, В.Н. Садовского, В.К. Финна. М.: Эдиториал УРСС, 2000.
- Лоун Б. Утерянное искусство врачевания/Пер. с англ. Е. Незлобиной. – М.:КРОН-ПРЕСС, 1998. 367 с.
- Нарский И.С. Современный позитивизм. М., 1961.
- Швырев В.С. Неопозитивизм и проблемы эмпирического обоснования науки. М., 1966.
- Якубик А. Познавательная ценность теории и учение об истерии (Источник – Интернет).
www.rusmedserv.com
Что такое верификация? | Простыми словами

В современном мире существует огромное количество разных терминов, которые появляются в огромном количестве каждый год. Стоит лишь немного не уследить за новшествами в какой-либо сфере, и всё – Вас завалят словами, значения которых Вы не знаете. В данной статье разберёмся, что такое верификация, говоря простыми словами.
Слово «верификация» происходит от двух латинских слов – verus (истинный) и facere (делать). Получается, что верификация – это процесс, который делает или подтверждает истинность чего-либо. Рассмотрим термин в различных сферах:
Верификация в философии – это установление истинности тех или иных теоретических утверждений на практике. Это же касается и «верификации» в науке.
Верификация в банке – это проверка личности клиента и предоставленных им данных. Дистанционные операции (например оплата покупки в интернете при помощи банковской карты) сопровождаются верификацией, которая, как правило, представляет из себя ввод отправленного по смс на телефон кода. То есть, вы подтверждаете, что покупку совершаете именно Вы, так как в своё время Вы уже подтвердили свой номер телефона.
Верификация в интернете – это подтверждение Вашей личности при регистрации в различных системах. К примеру, в социальных сетях пользователи, которые являются знаменитостями и имеют большое количество подписчиков, имеют синюю галочку. Это означает, что пользователь доказал, что это именно он является владельцем аккаунта с соответствующим именем.
Говоря простыми словами, верификация – это подтверждение или доказательство чего-либо. Если Вы говорите, что Вас зовут Иван Иванов, то верификацией станет, например, демонстрация паспорта, а если Вы снимаете деньги в банкомате, то подтвердить своё право на снятие наличных Вы можете при помощи пин-кода.
proslo.ru
Морфологическая верификация опухолей| Блог UNIM
Основная задача морфологической диагностики — установить тканевую принадлежность опухоли (гистогенез), при этом тщательно оценивается степень атипии самой клетки и нарушение тканевых структур. В большинстве случаев диагноз устанавливается по традиционно приготовленным препаратам, изучаемым при световой микроскопии. Для морфологического исследования используются различные методы забора материала:
— Соскобы и мазки-отпечатки. Являются распространенным способом диагностики поверхностных изъязвленных опухолей.
— Пункция. Выполняется при поверхностно расположенных узловых образованиях. При малых размерах подозрительных в отношении опухолевого роста образований возможно выполнение пункции под контролем УЗИ. В неясных случаях прибегают к проведению иммуногистохимических, электронно-микроскопических исследований, иногда выявляющих дополнительные морфологические признаки, позволяющие сопоставить опухоль с исходной тканью.В настоящее время при обнаружении опухоли внутренних органов возможно осуществить морфологическое исследование практически в любой части тела.
— Биопсия с забором участка ткани (браш-биопсия). Если пункцию выполнить невозможно, используют эндоскопические методы исследования: фаринго- и ларингоскопию, эзофагогастродуоденоскопию, торакоскопию, бронхоскопию, колоноскопию и др., в ходе которых под визуальным контролем обычно забирают участок ткани (биоптат или браш-биоптат — соскоб специальной щеточкой, смывы с поверхности образования и т.д.) для морфологического исследования.
— Открытая биопсия. Открытая биопсия опухоли выполняется, как правило, после неудачных попыток верифицировать диагноз вышеуказанными методами или из-за необходимости получить больше ткани для выполнения некоторых специфических исследований, например для определения рецепторов гормонов при опухолях молочной железы, иммуногистохимического исследования при гематосаркомах. Биопсия инцизионная предполагает получение участка ткани непосредственно из патологического очага, выполняется под местной анестезией (из опухоли молочной железы, мягких тканей) или под наркозом (из костных опухолей). Биопсия эксцизионная выполняется как хирургическое вмешательство с удалением опухоли в пределах здоровых тканей. Трепанобиопсия в основном используется для исследования новообразований молочной железы, костей, мягкотканных опухолей. При невозможности верифицировать злокачественность опухоли на диагностическом этапе планируют срочное гистологическое исследование во время операции.Эти способы обычно дают достаточно материала для морфологической верификации диагноза. Наиболее информативный материал получают из участков опухоли на границе со здоровой тканью.
— Трепан-биопсия. Гистологическая верификация может быть получена при использовании специальной иглы или трепана, при этом изымается столбик измененной ткани, пригодный для гистологического исследования. Особенно важным в плане адекватной диагностики распространенности опухолей бывает исследование сомнительных по клиническим данным образований в зонах регионарного метастазирования. В большинстве же случаев сопоставление клинических проявлений опухоли с ее симптомами вне основного очага не требует верификации всех обнаруженных метастазов. Производят морфологическое исследование наиболее доступных вторичных опухолей, что само по себе делает ясным представление об истинной распространенности заболевания. Верификация диагноза осуществляется путем чрезкожной пункции метастаза или забора материала при лапаро- или торакоскопии.
unim.su
